Casuistik 9
Der Fall
Es stellte sich einen 73 Jahre alte Frau mit Rücken-, Brustschmerzen und Atemnot vor.
Sie verspürte den Schmerz im Nacken, in der linken vorderen Brustwand und an der Seite des linken Oberbauches, die Beschwerden konnten weder durch die Körperhaltung provoziert werden noch waren sie atmungs- oder belastungsabhängig. Zusätzlich gab sie einen unproduktiven Husten und leichtes Pfeifen bei der Atmung an. Die Beschwerden traten intermittierend seit etwa 1 Woche auf, waren aber seit einigen Stunden sehr intensiv und mit Erbrechen verbunden. In der Vorgeschichte berichtete sie über eine seit etwa 20 Jahren unregelmäßig bekannte arterielle Hypertonie und eine ebenfalls seit Jahren bekannte COPD.
Die Frau war Nichtraucherin, beklagte keinen Gewichtsverlust und berichtete auch nicht über Schluckstörungen oder Hämoptysen.
Bei der Untersuchung stellte sich eine grazile schlanke Dame vor, die deutlich krank wirkte, wenn sie Brustschmerzen hatte und die gesund erschien, wenn sie beschwerdefrei war. Der Blutdruck wurde mit 140/80 mm Hg, die Herzfrequenz mit 104/min und die Temperatur mit 36°C gemessen. Bei einer Atemfrequenz von 20/min betrug die O2-Sättigung 96% unter 2 l Sauerstoff/min.
Das Atemgeräusch war beiderseits etwas abgeschwächt und man hörte ein leises spastisches Pfeifen über beiden Lungenspitzen.
Aufgrund der Intensität ihrer Beschwerden erhielt sie Morphium subkutan, wonach sie beschwerdefrei wurde; die Atemnot verbesserte sich unter Salbutamol.
Das Labor zeigte keine Auffälligkeiten: CRP und kleines Blutbild waren normal, das Kreatinin war normal und auch die d-Dimere nicht erhöht.
Abb. 1: EKG mit Zeichen der Linksherzhypertrophie |
Im EKG waren Zeichen der Linksherzhypertrophie ohne Schädigungszeichen oder andere Hinweise auf myokardiale Ischämien zu sehen.
Abb. 2: Echo mit Zeichen der Linksherzhypertrophie |
Im Echo waren die linksventrikulären Wände verdickt (IVS 15 mm), Aorten- und Mitralklappe kompetent und lediglich in der Aortenklappe waren geringe Kalzifikationen zu sehen.
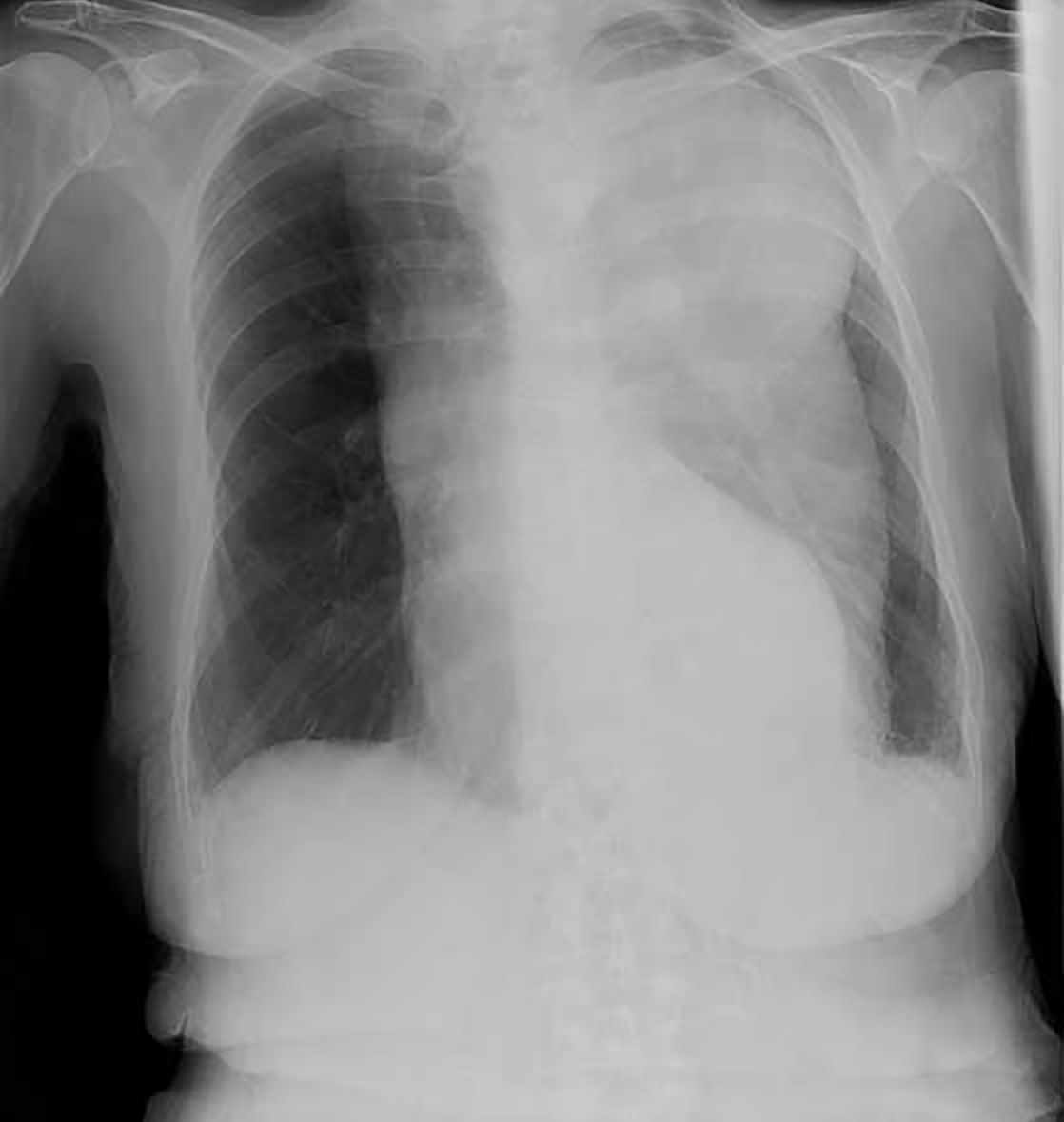 |
Abb. 3: Röntgenbild |
Das Röntgenbild (Abb. 3) zeigte eine massive Erweiterung der aszendierenden, deszendierenden Aorta und des Aortenbogens. Die Lungen waren etwas vermehrt strahlentransparent, ansonsten aber unauffällig.
Wie lautet die Diagnose?
Der betreuende Arzt vermutete ein thorakales Aortenaneurysma.
Der sofort konsultierte Kardiochirurg hielt eine Operation aber wegen ihrer COPD für sehr riskant und lehnte sie daher zunächst ab.
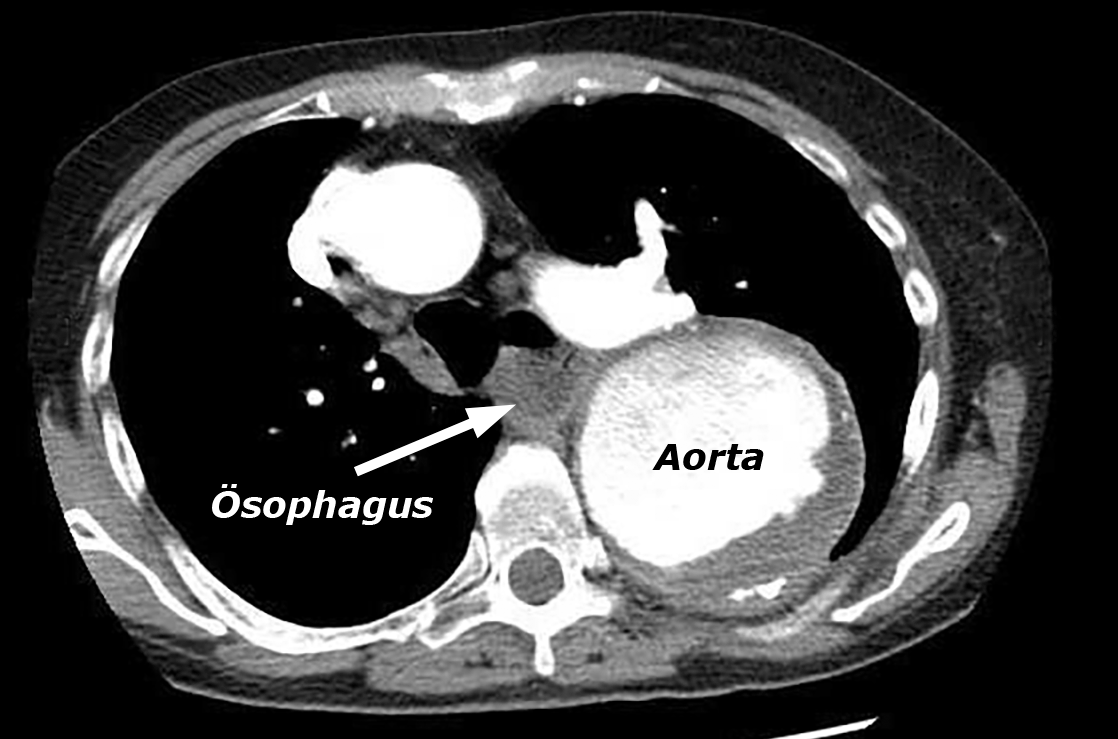 |
Abb. 4: Thorax-CT |
Im thorakalen CT sah man ein großes Aneurysma der aszendierenden thorakalen Aorta mit einem maximaler Durchmesser in Höhe der deszendierenden thorakalen Aorta von 8.5 cm. Eine Dissektion war nicht zu erkennen, links fand sich ein kleiner Pleurawinkelerguß, der im Röntgenbild nicht zu erkennen gewesen war.
Die Patientin wurde erneut dem Kardiochirurgen vorgestellt, der angesichts des Ausmaßes des Aneurysmas nun mit einer Operation einverstanden war, jedoch auf das erhöhte OP-Risiko hinwies.
Es wurde in allgemeiner Anästhesie ein 30 x 120 mm großer aortaler Stent implantiert.
Der Eingriff verlief komplikationslos, sodaß die Patientin am 15. postoperativen Tag entlassen werden konnte.
Die Ruptur oder Dissektion eines thorakalen Aortenaneurysmas tritt selten auf, hat aber eine hohe Mortalität. Daher ist es wichtig, eine solche Erkrankung schnell zu entdecken.
Bei der Mehrzahl der Patienten (ca. 75%) ist ein thorakales Aortenaneurysma asymptomatisch, Schmerzen treten bei ca. 15% aller Patienten auf. Die anderen Patienten können Brust- oder Nackenschmerzen, Heiserkeit infolge einer Kompression des N. recurrens, Schluckbeschwerden infolge der Kompression des Ösophagus oder Luftnot bei einer Kompression der Atemwege angeben.
Die CT-Untersuchung, die aufgrund des Röntgen-Thoraxbildes angefertigt wurde bestätigte nicht nur das thorakale Aortenaneurysma, sondern zeigte auch noch die Beteiligung der deszendierenden Aorta, was häufig auftritt. Die Untersuchung zeigte zudem eine gewisse Kompression des Ösophagus, ohne daß die Patientin Schluckstörungen angab.
Ein Aortenaneurysma kann sackförmig oder mehr diffus und unscharf (Aneurysma fusiforme) abgegrenzt sein und kann Ösophagus und/oder Trachea komprimieren.
Bei den „echten“ Aneurysmata (Aneurysma verum) sind alle Wandschichten der Aorta betroffen. Ursachen sind degenerative Erkrankungen der Gefäßwand (80% Atheriosklerose), stumpfe Traumata oder seltener auch Infektionen oder angeborene Bindegewebsschwächen.
Im Gegensatz dazu stehen Pseudoaneurysmata (Aneurysma falsum oder spurium). Sie entstehen in der Regel durch penetrierende Traumata. Dabei tritt Blut in die Adventitia oder das ein Gefäß umgebendes Gewebe aus, wo das Hämatom durch eine Bindegewebskapsel umgeben wird. Dieses Aneurysma falsum liegt somit außerhalb des eigentlichen Gefäßes.
In unserem Fall gab es weder eine genetische Disposition für das Auftreten des Aneurysmas noch systemische Erkrankungen, Hinweise auf Infektionen oder ein vorangegangenes Trauma.
Das CT zeigte einige atheromatöse Plaques in der Aorta, es ist aber nicht bekannt, ob arterioskleröse Aneurysmata durch solche Plaques verursacht werden oder ob die Plaques infolge struktureller Veränderungen einer aneurysmatischen Aorta entstehen. Man darf daher davon ausgehen, daß es sich um ein arteriosklerotisches Aneurysma handelte.
Bei solchen Aneurysmata sind Zigarettenrauchen, chronisch obstruktive Lungenerkrankung, fortgeschrittenes Lebensalter, Schmerzen, arterielle Hypertonie und ein Durchmesser des Aneurysma von >5 cm Faktoren, die das Risiko einer Ruptur erhöhen.
Im vorliegenden Fall konnte man aber trotz eines Durchmessers des Aneurysma von 8 cm, fortgeschrittenen Lebensalters und der arteriellen Hypertonie aufgrund der bislang nicht eingetretenen Ruptur von einer eher günstigen Prognose ausgehen. Dennoch war die Indikation zur operativen Therapie angesichts des Ausmaßes des Aneurysma natürlich gegeben.
Bezüglich der Operation gibt es in der Regel 2 Möglichkeiten:
- Ersatz der aneurysmatisch veränderten Aorta durch eine Dacron-Rohrprothese. Dabei hängt es von der Ausdehnung des Aneurysma ab, ob „lediglich“ das betroffene Aortenrohr ersetzt werden muß oder ob beim Befall der Aortenwurzel auch eine Bioprothese der Aortenklappe (z.B. in Form eines klappentragenden Conduits) implantiert werden muß. In diesen Fällen werden auch die Abgänge der Koronararterien in die Prothese implantiert werden müssen. Größter Nachteil solcher Operationen sind das in Abhängigkeit vom Umfang des Eingriffs hohe Komplikationsrisiko von bis zu 4 - 10%.
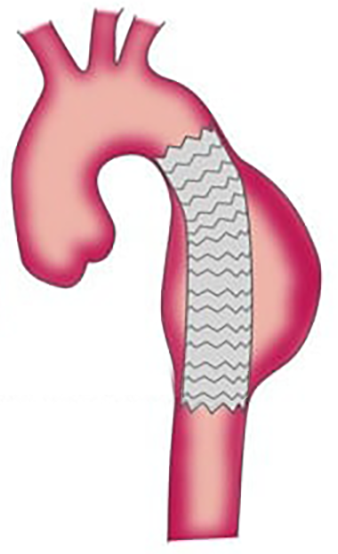
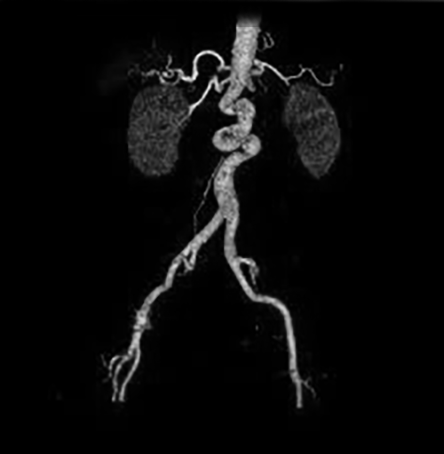
- Ein alternatives Verfahren ist die endovaskuläre Aneurysmatherapie (EAT oder EVAR für endovascular aneurysm bzw. aortic repair), bei der ein mit Kunststoff (Polyester oder PTFE) beschichteter Stent in das Aneurysma plaziert wird, sodaß das Aneurysma „ausgeschaltet“ wird (Abb. 5). Hauptproblem dieses Verfahrens sind sog. Endoleaks, also Leckagen, die in bis zu 44 % der Fälle auftreten können. Durch solche Leckagen kommt der Aneurysmasack wieder unter den systemischen Blutdruck, sodaß das Ziel der Operation nicht erreicht wird.